Rút ngắn thời gian phê duyệt thử nghiệm lâm sàng xuống 20 ngày, tạo cơ sở pháp lý cho việc ra mắt nhanh chóng các liệu pháp đột phá
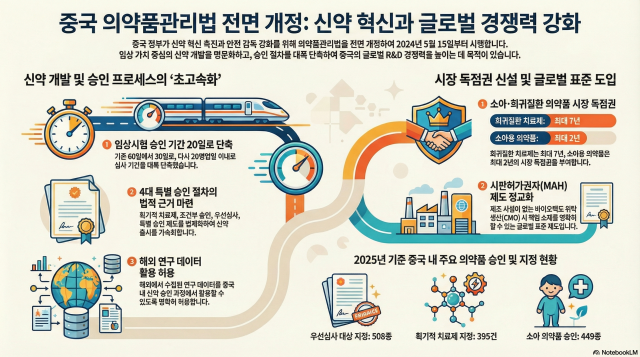
Chính phủ Trung Quốc đã cải cách toàn diện Luật Quản lý Dược phẩm sau 23 năm nhằm thúc đẩy đổi mới thuốc mới và tăng cường giám sát an toàn dược phẩm, dự kiến áp dụng từ ngày 15 tháng 5.
Theo tài liệu từ Hiệp hội Sinh học Hàn Quốc, sau các cải cách năm 2015 và 2019, lần này Trung Quốc đã tinh chỉnh cơ sở pháp lý cho toàn bộ chu kỳ phát triển thuốc mới. Điểm nổi bật là việc hợp pháp hóa phát triển thuốc mới hướng tới giá trị lâm sàng. Cơ quan Quản lý Dược phẩm Quốc gia (NMPA) có thể thực hiện chỉ định liệu pháp đột phá, phê duyệt có điều kiện, ưu tiên và đặc biệt với cơ sở pháp lý rõ ràng. Năm 2025, đã có 395 liệu pháp đột phá được chỉ định, 158 liệu pháp phê duyệt có điều kiện và 508 loại được ưu tiên xét duyệt.
Trung Quốc cũng thiết lập quyền độc quyền thị trường cho thuốc nhi và bệnh hiếm. Thuốc nhi có thể được độc quyền tối đa 2 năm, và thuốc bệnh hiếm tối đa 7 năm nếu đáp ứng điều kiện. Đến tháng 12 năm 2025, đã có 230 loại thuốc mới, 449 loại thuốc nhi và 170 loại thuốc bệnh hiếm được phê duyệt.
Thủ tục phê duyệt thử nghiệm lâm sàng được rút ngắn xuống còn 20 ngày làm việc. NMPA sẽ quyết định trong vòng 20 ngày sau khi nhận đơn. Điều này tiếp tục rút ngắn từ 60 ngày xuống 30 ngày vào tháng 9 năm ngoái. Dữ liệu nghiên cứu từ nước ngoài được phép sử dụng tại Trung Quốc, và giám sát bán hàng, sản xuất trực tuyến cũng được tăng cường.
Ngành dược phẩm sinh học cho rằng cải cách này sẽ tăng tốc độ phát triển thuốc mới, nâng cao năng lực cạnh tranh R&D toàn cầu của Trung Quốc. Trong bối cảnh Mỹ và châu Âu thắt chặt hợp tác nghiên cứu, Trung Quốc đang tìm cách mở rộng hợp tác toàn cầu và xuất khẩu công nghệ thông qua hệ thống quy định trưởng thành hơn.
Đặc biệt, hệ thống MAH giúp làm rõ trách nhiệm khi các công ty công nghệ sinh học không có cơ sở sản xuất tự giao cho CMO sản xuất, đã được áp dụng tại châu Âu, Mỹ và Nhật Bản. Trong khi đó, Hàn Quốc vẫn chưa áp dụng quy định MAH, dẫn đến sự không rõ ràng về quản lý chất lượng và trách nhiệm giữa nhà phát triển và nhà sản xuất gia công. Cải cách của Trung Quốc được kỳ vọng sẽ nâng cao năng lực cạnh tranh của hệ sinh thái phát triển thuốc mới.
* Bài viết này được dịch tự động bằng AI.














![[Xã Luận] Tương lai châu Á qua lăng kính IMF: Từ cạnh tranh bá quyền công nghệ đến lộ trình cùng phát triển giữa Hàn Quốc và Trung Quốc](https://image.ajunews.com/content/image/2026/02/20/20260220142908584761_518_323.png)